تعریف اسید
«اسید»، از اصطلاحات مهم علم شیمی است که در میان عموم، به موادی ترش مزه اطلاق میشود که در برخی خوراکی ها و مواد غذایی نظیر سرکه و آب مرکبات یافت میشوند. خاصیت خوندگی دارند و در صورت تماس با پوست و سایر اعضاء بدن التهاب و سوزش ایجاد میکنند و از این رو میتوانند خطرناک نیز باشند. در بعد علمی، واژه ی لاتین Acid توسط هر یک از دانشمندان به شکلی متفاوت تعریف شده است.
در ادامه با تعاریف این اصطلاح و ویژگی های کلی اسیدها آشنا میشویم.
اسید چیست؟
این واژه از Acidus برگرفته شده که به معنای ترشی است. در گذر زمان، دانشمندان تعاریفی متفاوت از اصطلاح اسید ارائه کرده اند.
از دیدگاه لی بیگ، اسیدها موادی هستند که در ترکیب شیمیایی خود دارای اکسیژن بوده و در اثر واکنش با فلزات، توسط یون های فلز جایگزین میگردند.
برونستد و لوری، لفظ اسید را به موادی اطلاق میکنند که قابلیت اهدای پروتون را دارا هستند. بر اساس این تعریف، الکل ها و آمین ها نیز در دسته ی مواد اسیدی جای میگیرند. تعریف برونستد و لوری، به نسبت سایر تعاریف متداول تر میباشد.
تعریف اسید از آرنیوس:
طبق تعریف آرنیوس، اسیدها موادی هستند که در آب، یون هیدروژن آزاد میکنند. البته این یون به صورت آزاد باقی نمیماند و به سرعت به یون هیدرونیوم (+H3O) تبدیل میشود. در نتیجه، وجود اسید در آب، سبب افزایش غلظت یون هیدرونیوم خواهد شد.
تلاش های آرنیوس برای شناخت بهتر اسیدها و ارائه ی تعاریف دقیقتر از آنها، جایزه ی نوبل شیمی را برای او به ارمغان آورد.
تعریف اسید از زبان لوییس:
لوییس اصطلاح اسید را برای موادی به کار میبرد که در پی دریافت دو الکترون، پیوند کوالانسی ایجاد میکنند. بر اساس این تعریف و بر خلاف نظر پیشینیان، حتی برخی از مواد شیمیایی فاقد هیدروژن نیز اسید محسوب میشوند.
ویژگی های اسید ها
اسیدها طعمی ترش دارند و بسیار خورنده اند. از این رو میتوانند سبب آسیب رساندن به فلزات و مواد دیگر شوند. به علاوه، بسیاری از اسیدهای قوی برای انسان خطرناک هستند و در صورت تماس با آنها، التهاب، زخم یا سوزش ایجاد میشود. اسیدها از نظر بار الکتریکی خنثی هستند و در پی انحلال در آب، خاصیت رسانایی الکتریکی پیدا میکنند.
انواع اسیدها
از نظر قدرت: موادی که در دسته ی اسیدها قرار میگیرند از نظر میزان قدرت و خاصیت اسیدی با یکدیگر متفاوت اند.
برخی از آنها در نتیجه ی انحلال در آب، به طور کامل پروتون هایشان را اهدا میکنند و غلظت یون هیدرونیوم را به شدت افزایش میدهند. به عبارت بهتر، قدرت تفکیک پذیری بسیار بالایی دارند. این نوع اسیدها، نسبت به سایرین قوی تر میباشند. مانند: نیتریک اسید، سولفوریک اسید و کلریدریک اسید
در مقابل برخی از مواد اسیدی، واکنش شدیدی ایجاد نمیکنند و در پی انحلال در آب، پروتون هایشان را به طور کامل از دست نمیدهند و کاملا تفکیک نمیشوند. این مواد، خاصیت اسیدی ضعیف تری دارند. اغلب اسیدهای ضعیف، از نوع مواد آلی هستند. مانند: لاکتیک اسید، سیتریک اسید و استیک اسید

انواع اسید ها از نظر ترکیب شیمیایی:
اسیدهای دوتایی (Binary Acids): این نوع اسیدها در ترکیب خود حاوی اتم دو عنصر هیدروژن و یک نافلز هستند. اسیدهای باینری در نتیجه ی انحلال در آب، یون هیدروژن از دست میدهند.
اکسواسیدها (Oxoacid): در اکسواسیدها، پیوند اتم هیدروژن با عنصر نافلز، از طریق یک اتم اکسیژن اتفاق می افتد. بنابراین، این نوع اسیدها دست کم از یک اتم اکسیژن و یک اتم هیدروژن برخوردار هستند.
تیواسیدها (TheoAcid): در مواردی که به جای یک یا چند اتم اکسیژن اکسواسید، اتم های گوگرد در ساختار ماده موجود باشند، با تیواسیدها مواجه هستیم.
از نظر منشاء: اسیدها با توجه به منشاء شان به دو دسته ی آلی و معدنی تقسیم بندی میشوند.
اسیدهای آلی: این گروه از اسیدها از مواد آلی به دست می آیند که خود به چند دسته تقسیم میشوند. مهم ترین گروه اسیدهای آلی، کربوکسیل اسیدها هستند. این نوع اسیدها غالبا ضعیف میباشند. اسیدهای آلی در انواع محصولات گیاهی یافت میشوند و برخی از آنها در بدن جانوران تولید میشوند.
اسیدهای معدنی: ترکیبات اینچنینی از مواد معدنی مانند فلزات به دست آمده و فاقد کربن هستند.
تعریف بازها
باز (BASE) درست نقطه ی مقابل اسید است. این مواد، بر اساس سه تعریف گوناگون، دریافت کننده ی پروتون، کاهش دهنده ی غلظت یون هیدرونیوم در آب و افزایش دهنده ی یون های هیدروکسید میباشد.
بازها مزه ی تلخی دارند و بسیار لغزنده اند. در تماس با دست حالت صابونی ایجاد میکنند و همچنین با اسیدها واکنش داده، آن را خنثی کرده و در پی آن آب و نمک تولید میکنند.
تشخیص میزان اسیدی بودن مواد
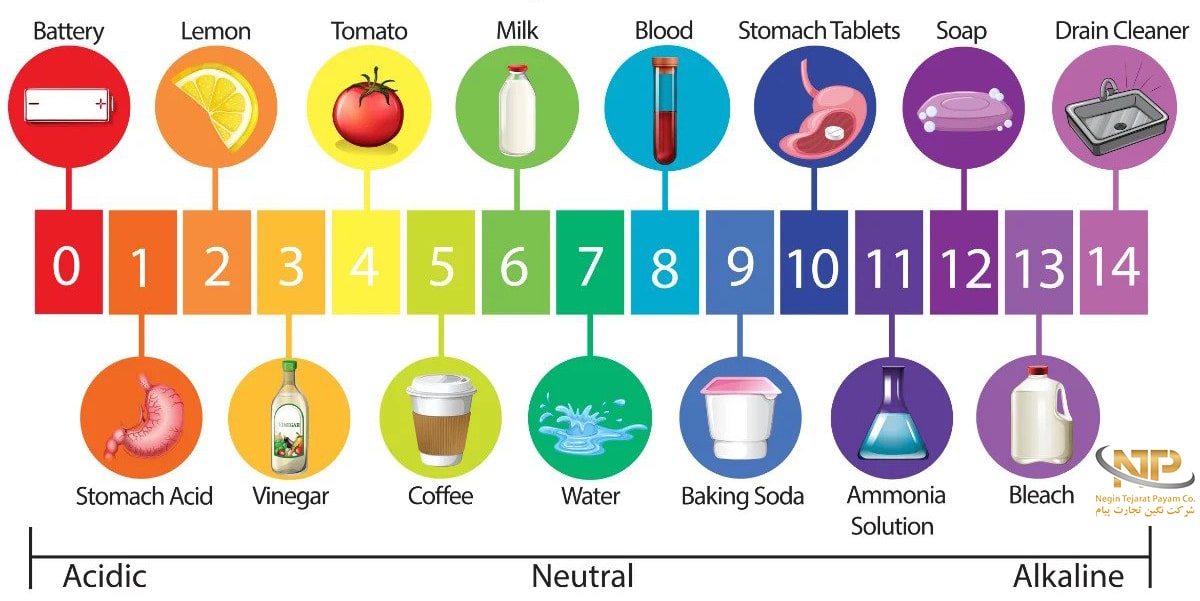
به طور کلی برای تشخیص اسیدها از بازها و تعیین میزان قدرت هر یک، از مقیاسی به نام pH استفاده میشود. pH بازه ای از ۰ تا ۱۴ را در بر میگیرد که در آن اعداد کوچکتر از ۷ نمایانگر اسیدها هستند و هر چه به ۷ نزدیکتر باشند خاصیت اسیدی ضعیفتری را نشان میدهند. در مقابل، اعداد بزرگتر از ۷ معرف بازها میباشند و هر چه به ۱۴ نزدیکتر باشند نشانگر بازهای قوی تری هستند. pH هفت و نزدیک به آن نیز به مواد خنثی مانند آب مربوط میباشد که در هیچ یک از دو دسته ی اسید و باز نمیگنجند.
برای تعیین خاصیت اسیدی یا قلیایی مواد، از انواع شناساگرها استفاده میشود که مشهورترین آنها کاغذ تورنسل یا لیتموس است.
کاغذ تورنسل یا لیتموس که از گل سنگ ساخته میشود، در مواجهه با اسیدها و بازها تغییر رنگ داده و به طور کلی، طیفی از رنگ های آبی تا قرمز را از خود نشان میدهد. در محیط های اسیدی به رنگ قرمز و در محیط های بازی به رنگ آبی در می آید. اسیدهای قوی را به رنگ قرمز تیره و بازهای قوی را به رنگ آبی تیره نمایان میکند. مواد خنثی یا نسبتا خنثی نیز کاغذ تورنسل را به رنگ بنفش در می آورند.
این کاغذ به دو رنگ آبی و قرمز یافت میشود. کاغذ تورنسل آبی برای تشخیص میزان خاصیت اسیدی و کاغذ تورنسل قرمز برای تشخیص قدرت بازها به کار میرود.
برای استفاده از این شناساگر، ابتدا چند قطره از محلول را بر روی آن میریزند. البته در مواردی نیز کاغذ را به درون محلول فرو میبرند که روش مناسبی نمیباشد، چراکه تمام محلول را آلوده خواهد کرد. پس از آن، منتظر میمانند تا کاغذ تورنسل تغییر رنگ دهد و بر اساس راهنمای طیف رنگها، میزان pH یا خاصیت اسیدی و قلیایی آن مشخص میشود.
شیوه ی نام گذاری اسیدها:
برای نام گذاری اسیدها از نام نافلزهای آنها استفاده میکنیم.
در خصوص اکسواسیدها، پسوند (ییک+اسید) به نام اتم مرکزی افزوده میشود. مانند: فسفریک اسید یا نیتریک اسید. البته در برخی موارد اتم مرکزی مورد نظر بیش از یک نوع اکسواسید تولید میکند که تعداد اتم های اکسیژن هرکدام با دیگری متفاوت است. در این موارد، نام اسیدی که ظرفیت اتم مرکزی آن یک مرتبه از حالت معمول کمتر است با پسوند (و+اسید) مشخص میشود. مانند: سولفورو اسید و فسفرو اسید.
اگر تعداد اتم ها دو مرتبه از حالت معمول کمتر شود، پیشوند (هیپو) میگیرد. مثل: هیپوفسفرواسید. اگر تعداد اتم های اکسیژن اکسواسید، از حالت عادی یک عدد بیشتر باشد، پیشوند (پر) به آن افزوده خواهد شد. مانند: پرکلرواسید.
برای نامگذاری اسیدهای باینری یا دوتایی، پیشوند (هیدرو) را به نام نافلز آن می افزاییم و پسوند (ییک+اسید) را نیز به آن اضافه میکنیم. مثل: هیدروکلریک اسید (خرید هیدروکلریک اسید).
نام اسیدهای آلی نیز در نتیجه ی افزودن پسوند (ییک+اسید) به نام آلکان تشکیل دهنده شان ساخته میشود. مانند: فرمیک اسید و سیتریک اسید.
در مورد تیواسیدها، پسوند (ییک+اسید) و پیشوند (تیو) به آنها اضافه میشود . بر اساس تعداد اتم های گوگرد موجود در ترکیب شیمیایی شان، پیشوند (دی) یا (مونو) میگیرند. مثل: مونوتیو فسفریک اسید و تیو سولفوریک اسید.
کاربرد های اسید
اسیدها در صنعت و زندگی روزمره ی ما کاربردهای فراوانی دارند.
- بسیاری از اسیدها مانند سیتریک اسید و استیک اسید، به علت طعم ترششان به عنوان افزودنی غذایی مورد استفاده قرار میگیرند.
- از برخی اسیدها برای خنثی سازی و تنظیم میزان PH خاک یا محلول های قلیایی استفاده میشود.
- بعضی اسیدها مانند سولفوریک اسید و اسید فسفریک به عنوان کود به خاک مزارع کشاورزی افزوده میشوند تا ضمن کاهش PH خاک، عناصر ضروری مورد نیاز گیاهان را تأمین نمایند.
- در صنعت و آزمایشگاه های شیمی، از اسیدها به عنوان کاتالیزور استفاده میشود.
- برای تهیه ی نمک، انواع گوناگون اسیدها را مورد استفاده قرار میدهند تا در نتیجه ی واکنش با نوع مشخصی از بازها، نمک تولید نمایند.
- به عنوان الکترولیت در سلول های باتری مورد استفاده قرار میگیرند. مانند: سولفوریک اسید یا جوهر گوگرد
- به عنوان مواد نگهدارنده و مکمل های غذایی به کار میروند.
- حضور انواع گوناگون اسیدها در بدن انسان ضروری است. به عنوان مثال اسیدها برای هضم غذا در معده و تولید پروتئین نقش دارند.
- در بسیاری از موارد برای رسوب زدایی و جرم گیری سطوح گوناگون کارایی دارند.
- برخی از آنها به عنوان لعاب برای پوشاندن سطوح به کار میروند.
- از برخی اسیدها در تهیه ی مهمات نظامی و مواد منفجره استفاده میشود مانند نیتریک اسید یا جوهر شوره
- بسیاری از اسیدها مانند اسید لاکتیک و اگزالیک اسید در صنعت نساجی به کار میروند.
- از اسید فلوریدریک برای ساخت آثار هنری با شیشه و تعیین اصالت برخی از آثار اینچنینی استفاده میشود.
- بسیاری از اسیدها مانند اسید فرمیک، به عنوان مواد ضدعفونی کننده مورد استفاده قرار میگیرند.

